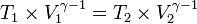Rumus-Rumus Fisika
Termodinamika
Hukum Pertama Termodinamika
Perubahan energi dalam:
Keterangan:
 :Perubahan energi dalam (Joule)
:Perubahan energi dalam (Joule)- U2:Energi dalam pada keadaan akhir (Joule)
- U1:Energi dalam pada keadaan awal (Joule)
- p: Besarnya tekanan (atm)
 : Perubahan volume (liter)
: Perubahan volume (liter)

Penghitungan energi dalam:
- Gas monoatomik:

- Gas diatomik:

Proses-proses termodinamika gas
Proses isobarik
Diagram proses isobarik. Daerah berwarna kuning sama dengan usaha yang dilakukan.
Persamaan keadaan isobarik:
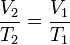
Usaha yang dilakukan pada keadaan isobarik:

Proses isokhorik
Digram proses isokhorik. Grafiknya berupa garis lurus vertikal karena
volumenya tidak berubah. Tidak ada usaha yang dilakukan pada proses
isokhorik.
Persamaan keadaan isokhorik:

Proses isotermis/isotermik
Proses isotermik. Daerah berwarna biru menunjukkan besarnya usaha yang dilakukan gas.
Persamaan keadaan isotermik:
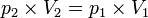
Usaha yang dilakukan pada keadaan isotermik:
- Dari persamaan gas ideal

- Rumus umum usaha yang dilakukan gas:

maka:

karena
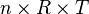 bernilai tetap, maka:
bernilai tetap, maka:
Ingat integral ini!

maka persamaan di atas menjadi
Proses adiabatik
Proses adiabatik. Warna biru muda menunjukkan besarnya usaha yang dilakukan.
Persamaan keadaan adiabatik:

Tetapan Laplace:
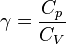
karena
 , maka persamaan diatas dapat juga ditulis:
, maka persamaan diatas dapat juga ditulis:

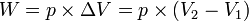



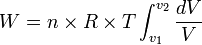
![W = n \times R \times T \times[\ln V_2 - \ln V_1]](https://upload.wikimedia.org/math/0/a/7/0a71834fa480baf975b62a9a64bb7b7d.png)